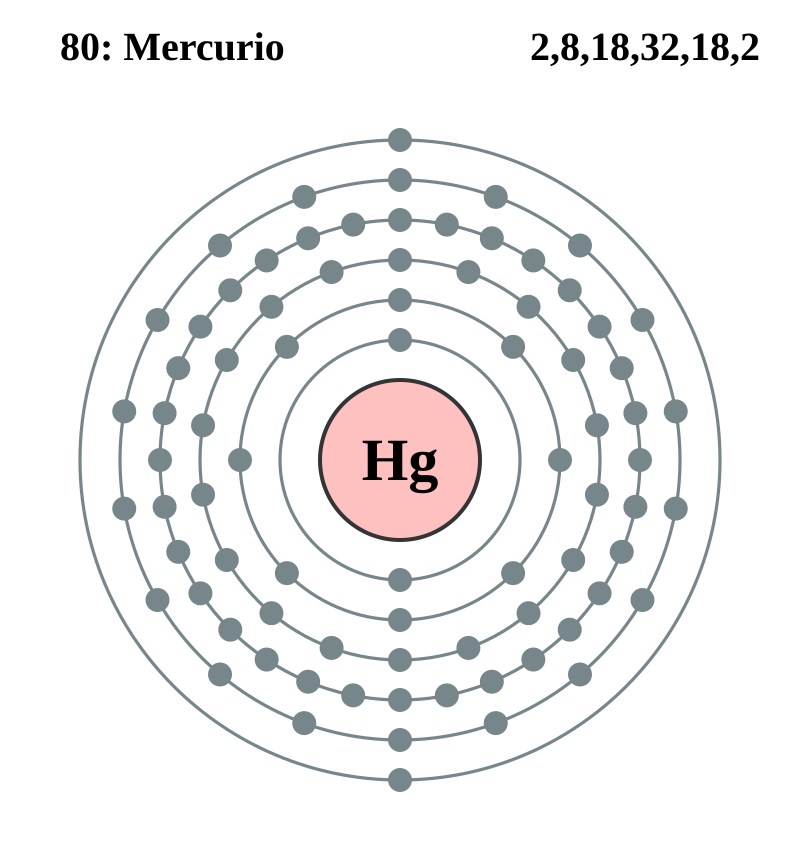
Elemento de aspecto plateado,El mercurio es un elemento químico con el Hg y número atómico80.
En la literatura antigua era designado comúnmente como plata líquida y también como azogue o hidrargiro.1
- metal pesado perteneciente al bloque D de la tabla periódica,
- el mercurio es el único elemento metálico que es líquido en condiciones estándar de laboratorio;
- El mercurio aparece en depósitos en todo el mundo, principalmente como cinabrio (sulfuro de mercurio).
- El pigmento rojo denominado bermellón se obtiene triturando cinabrio natural.
USOS DEL MERCURIO:
- El mercurio se usa en termómetros,
- barómetros,
- manómetros,
- la preocupación sobre la toxicidad del elemento ha llevado a los termómetros y tensiómetros de mercurio a ser eliminados en gran medida en entornos clínicos en favor de otras alternativas, como los termómetros de vidrio que utilizan alcohol
- algunos tipos de válvulas como las de las bombas de vacío,
- interruptores de mercurio,
- lámparas fluorescentes
- El mercurio se mantiene en uso en aplicaciones de investigación científica
- y en amalgamas odontológicas,
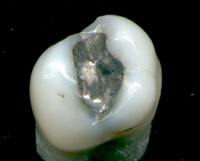
- todavía utilizadas en algunos países.
- El mercurio también se utiliza en los telescopios de espejo líquido.Algunos telescopios utilizan un recipiente con mercurio para formar un espejo plano y absolutamente horizontal
- El cloruro de mercurio se ha utilizado en la medicina tradicional como diurético, desinfectante tópico, y laxante.
- También se utiliza como desinfectante. El "Blue mass", una pastilla o jarabe en el que el mercurio es el ingrediente principal, se recetó a lo largo del siglo XIX para numerosas enfermedades, como el estreñimiento, la depresión, la infertilidad y los dolores de cabeza.93
- A principios del siglo XX, el mercurio se administró a niños pequeños como laxante y vermífugo, y se utilizó en polvo dental para lactantes.
- También se utiliza en las luces fluorescentes, en las que la electricidad que atraviesa una lámpara conteniendo vapor de mercurio produce radiación ultravioleta , que a su vez provoca la fluorescencia del fósforo que recubre el tubo, produciendo luz visible.
Usos históricos[editar]
Muchas aplicaciones históricas hacen uso de las peculiares propiedades físicas del mercurio, sobre todo como un líquido denso y como un metal líquido:
- Cantidades de mercurio líquido de entre 90 y 600 g han sido recuperadas de tumbas de las élites de la civilización maya (entre los años 100 y 700)71 o en vasijas rituales en seis lugares. Este mercurio pudo haber sido utilizado en cuencos como espejo con fines adivinatorios. Cinco de ellos datan del período clásico de la civilización maya (c. 250-900), pero uno de los seis ejemplos es anterior.72
- Fue utilizado como colorante en forma de bermellón (cinabrio en polvo), formando parte de forma extensiva de las pinturas de color rojo durante siglos, hasta ser sustituido por el rojo de cadmio (que no es tóxico).
- En la España Islámica fue utilizado para llenar piscinas decorativas. Siglos después, el artista estadounidense Alexander Calder construyó una fuente de mercurio para el Pabellón Español de la Exposición Internacional de París de 1937. La fuente está ahora en exhibición en la Fundació Joan Miró en Barcelona.73
- El mercurio se utilizaba dentro de señuelos de pesca oscilantes. Su forma pesada, con la inestabilidad propia del mercurio líquido en su interior, hace que el movimiento irregular de estos señuelos sea muy atractivo para los peces. Su uso se prohibió por motivos ambientales, pero se ha producido la posterior reaparición de este arte de pesca ilegal.
- Las lentes de Fresnel de los faros antiguos utilizaban un baño de mercurio sobre el que flotaban y rotaban, actuando como un cojinete.74
- En los primeros años de la radiodifusión a comienzos del siglo XX, para generar ondas hercianas con frecuencias de kilociclos, se utilizaban unos interruptores electromecánicos consistentes en una rueda dentada metálica que interceptaba un flujo continuo de mercurio por el que se hacía circular la electricidad (véase Conectores de mercurio).
- Esfigmomanómetros (medidores de presión arterial), barómetros, bombas de difusión, coulombímetros, y otros muchos instrumentos de laboratorio utilizan mercurio. Como líquido opaco con una alta densidad y una expansión térmica casi lineal, es ideal para este uso.75
- Como líquido conductor de la electricidad, se utilizó en interruptores de mercurio (incluyendo algunos tipos de interruptores de luz domésticos instalados antes de 1970), interruptores basculantes utilizados en detectores de fuego antiguos, y los interruptores de inclinación de algunos tipos de termostatos domésticos.76
- Debido a sus propiedades acústicas, el mercurio se utilizó como medio de propagación en dispositivos con memoria de línea de retardo utilizados en las primeras computadoras digitales de la mitad del siglo XX.
- Turbinas de vapor de mercurio experimentales se instalaron para aumentar la eficiencia de la energía eléctrica de las plantas de combustibles fósiles.77 La planta de energía South Meadow en Hartford (Connecticut), empleó mercurio como fluido de trabajo (en una configuración binaria con un circuito de agua secundario) durante una serie de años a partir de finales de la década de 1920, en un intento por mejorar la eficiencia de la planta. Varias otras plantas fueron construidas con este diseño de turbina, incluyendo la estación Schiller en Portsmouth (Nuevo Hampshire) que se puso en servicio en 1950. La idea no tuvo éxito en toda la industria debido al peso y a la toxicidad del mercurio, así como a la aparición de las plantas de vapor supercrítico en los años siguientes.7879
- Del mismo modo, el mercurio líquido se utilizó como refrigerante para algunos reactores nucleares; sin embargo, el sodiose ha impuesto para los reactores enfriados con metal líquido, debido a que la alta densidad del mercurio requiere mucha más energía para hacerlo circular por los circuitos de refrigeración.80
- El mercurio era un propulsor de motores iónicos en los inicios de los sistemas de retropropulsión espacial eléctrica. Sus ventajas eran su alto peso molecular, su baja energía de ionización, su baja energía de doble ionización, la alta densidad del líquido y la capacidad de almacenamiento del metal a temperatura ambiente. Sus desventajas eran los problemas relacionados tanto con impactos ambientales asociados con las pruebas, como con el eventual enfriamiento y condensación de algunos de los propelentes en la nave espacial en las operaciones de larga duración en tierra. El primer vuelo espacial que utilizó la propulsión eléctrica con un propulsor de iones de mercurio como combustible (desarrollado por el centro de investigación NASA Lewis) fue la nave espacial "SERT-1" lanzada por la NASA en 1964. El vuelo SERT-1 fue seguido por el SERT-2 en 1970. El mercurio y el cesio fueron los propulsores utilizados en los primeros motores de iones, hasta que en el Hughes Research Laboratory se descubrió que el gas xenón es un sustituto más adecuado. El xenón es ahora el propelente utilizado en los motores de iones, ya que tiene un alto peso molecular, poca o ninguna reactividad debido a su naturaleza de gas noble, y presenta una alta densidad cuando se almacena como un líquido a baja temperatura.8182
Otras aplicaciones hacen uso de las propiedades químicas del mercurio:
- La batería de mercurio es un tipo de acumulador eléctrico no recargable, una celda primaria muy común a mediados del siglo XX. Se utilizaba en una amplia variedad de aplicaciones y estaba disponible en varios tamaños, en particular para las pequeñas pilas botón. Su salida de tensión constante y larga vida útil le dieron un uso específico en los medidores de luz las cámaras fotográficas y en los audífonos. Las pilas de mercurio fueron prohibidas de manera efectiva en la mayoría de los países en la década de 1990, debido a las preocupación por la contaminación por mercurio del suelo.83
- El mercurio se utiliza para la conservación de la madera, la creación de daguerrotipos, el plateado de espejos, en pinturas navales para evitar que se adhieran distintos organismos al casco de los buques (uso abandonado en 1990), herbicidas(abandonado en 1995), pequeños juguetes en forma de laberintos de bolsillo en los que se debe guiar una gota de mercurio, algunos productos de limpieza, y en los sensores de algunos dispositivos de suspensión autonivelante utilizados en su momento en automoción. Como medicamentos, los compuestos de mercurio se han utilizado en antisépticos, laxantes, antidepresivos, y en tratamientos contra la sífilis.
- Supuestamente fue utilizado por espías de los Aliados en acciones de sabotaje contra la Luftwaffe, mediante una pasta de mercurio que provocaba la rápida corrosión del aluminio de los aviones, causándoles fallos estructurales graves.84
- Proceso cloroálcali: El principal uso industrial del mercurio durante el siglo XX fue en la electrólisis para separar el cloro y el sodio de la salmuera; sirviendo el mercurio como ánodo del proceso Castner-Kellner. El cloro se utiliza para el blanqueo de papel (por lo que la localización de muchas de estas plantas estaba cerca de fábricas de papel), mientras que el sodio se utiliza para fabricar hidróxido de sodio utilizado en jabones y otros productos de limpieza. Este uso ha sido abandonado en gran medida, sustituyéndose por otras tecnologías que utilizan membranas osmóticas.85
- Como electrodos en algunos tipos de electrólisis, en catalizadores y en insecticidas.
- El mercurio también fue utilizado como limpiador del interior de los cañones de las armas de fuego.8687
- A partir de mediados del siglo XVIII hasta mediados del siglo XIX, se utilizó en la fabricación de sombreros de fieltro un proceso denominado "carroting". Las pieles de animales eran lavadas en una solución de nitrato mercúrico (Hg (NO32H2O2) de color naranja (el término "carroting", de zanahoria en inglés, surgió de este color).88 Este proceso separa la piel del pelaje enmarañado, aunque esta disolución y los vapores que produce son altamente tóxicos. El Servicio de Salud Pública de los Estados Unidos prohibió el uso de mercurio en la industria del fieltro en diciembre de 1941. Los síntomas psicológicos asociados con el envenenamiento por mercurio inspiraron la expresión inglesa "mad as a hatter"(loco como un sombrerero). El personaje de El Sombrerero de Lewis Carroll en su libro Las aventuras de Alicia en el país de las maravillas era un juego de palabras basado en la antigua frase, pero el carácter mismo del personaje no presenta síntomas de envenenamiento por mercurio.89
- Minería de oro y plata. Históricamente, se utilizó mercurio ampliamente en minería hidráulica con el fin de separar por flotación el oro (que se hunde en el mercurio) de la mezcla de grava y de agua que lo acompañan. Las partículas finas de oro además pueden formar una amalgama mercurio-oro y, por lo tanto, aumentar los porcentajes de recuperación de oro.5 El uso a gran escala del mercurio se detuvo en la década de 1960. Sin embargo, se sigue utilizando a pequeña escala, a menudo clandestina, en la prospección de oro. Se estima que 45.000 toneladas métricas de mercurio que fueron utilizadas en California en la explotación de placeres auríferos no han sido recuperadas.90 Mercurio fue también usado en plata mining.91
ENVENENAMIENTO POR MERCURIO
El envenenamiento por mercurio puede resultar de
- la exposición a las formas solubles en agua del mercurio ,
- por la inhalación de vapor de mercurio,
- o por la ingestión de cualquiera de sus formas.(WIKI)
- El mercurio puede ser absorbido por la piel y las membranas mucosas y los vapores de mercurio puede ser inhalados accidentalmente, por lo que los contenedores de mercurio estén bien sellados para evitar derrames y evaporación.
- El calentamiento del mercurio o de sus compuestos, que pueden descomponerse cuando se calientan, debe llevarse a cabo con una ventilación adecuada a fin de minimizar la exposición al vapor de mercurio.
- . El mercurio puede causar tanto intoxicaciones crónicas como agudas, incluyendo el envenenamiento por mercurio.
- La exposición crónica afecta principalmente al sistema nervioso central y a los riñones. La nefrotoxicidad se debe a la alta afinidad entre los iones mercúricos y los grupos sulfhidrilos (-SH) reducidos, los conjugados mercúricos con albúmina, L-cisteína, homocisteína y glutatión son las formas biológicamente importantes de Hg2+ en circulación.96
- Los efectos nocivos del mercurio pueden ser transmitidos de la madre al feto, e incluyen daño cerebral, retraso mental, falta de coordinación, ceguera, convulsiones e incapacidad para hablar. Los niños con envenenamiento por mercurio pueden desarrollar problemas en sus sistemas nervioso y digestivo y daños renales.12
- El envenenamiento por mercurio (también conocido como hidrargiria, hidrargirismo o mercurialismo) es una enfermedad causada por la exposición al mercurio o sus compuestos. Los efectos tóxicos incluyen daños al cerebro, los riñones y los pulmones. El envenenamiento por mercurio puede provocar varias enfermedades, incluyendo acrodinia (enfermedad rosada), el síndrome de Hunter-Russell, y la enfermedad de Minamata.
- Los síntomas suelen incluir discapacidad sensorial (visión, audición, habla), sensación alterada y la falta de coordinación. El tipo y el grado de síntomas que presenten dependen de la toxina individuales, la dosis, y el método y duración de la exposición.
| Mercurio → Talio | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tabla completa • Tabla ampliada | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Gotas de mercurio en un frasco. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Información general | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nombre, símbolo, número | Mercurio, Hg, 80 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Serie química | Metales de transición | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo, período, bloque | 12, 6, d | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa atómica | 200,59 u | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuración electrónica |
Completa: 1s²2s²2p63s²3p64s²3d104p65s² 4d10 5p66s²4f145d10
Abreviada: [ Xe] 4f14 5d10 6s² | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureza Mohs | 1,5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electrones por nivel | 2, 8, 18, 32, 18, 2 (imagen) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades atómicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio medio | 150 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegatividad | 2,00 (escala de Pauling) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio atómico(calc) | 171 pm (radio de Bohr) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio covalente | 149 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio de van der Waals | 155 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estado(s) de oxidación | 4, 2, 1 (levemente básico) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1.ª Energía de ionización | 1007,1 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2.ª Energía de ionización | 1810 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3.ª Energía de ionización | 3300 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades físicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estado ordinario | Líquido | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densidad | 13534 kg/m3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto de fusión | 234,32 K (-39 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto de ebullición | 629,88 K (357 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpía de vaporización | 59,229 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpía de fusión | 2,295 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Presión de vapor | 0,0002 Pa a 234 K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Varios | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estructura cristalina | Romboédrica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N° CAS | 7439-97-6 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor específico | 140 J/(K·kg) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductividad térmica | 8,34 W/(K·m) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocidad del sonido | 1407 m/s a 293,15 K (20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isótopos más estables | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Artículo principal: Isótopos del mercurio | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Valores en el SI y condiciones normales de presión y temperatura, salvo que se indique lo contrario. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| [editar datos en Wikidata] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

.JPG/800px-Cinabre_et_billes_de_mercure_natif_(Espagne).JPG)








Comentarios
Publicar un comentario